近日,一项发表于《中国肿瘤生物治疗杂志》的研究(2025年5月),首次系统对比了同立海源 ActSep® CD3/CD28分选激活磁珠与知名进口品牌磁珠在CAR-T制备中的性能差异。结果令人振奋:国产磁珠不仅达到与进口品牌相当的水平,更在多项关键指标上实现超越!

CAR-T细胞疗法凭借在血液肿瘤治疗中的惊艳疗效,成为全球生物医药领域的 “明星赛道”。截至 2025年8月,国内外已有十余款 CAR-T 药物上市,千余种候选药物进入研发阶段——但在这一“抗癌利器”的制备过程中,藏着一个关键的 “卡脖子” 环节:CAR-T细胞制备关键原料磁珠,长期高度依赖进口。

T细胞激活是CAR-T制备的核心步骤 ——只有通过CD3(信号1)和CD28(信号2)双信号刺激,T 细胞才能被有效激活、增殖,进而被改造成能精准杀瘤的CAR-T细胞。目前,CD3/CD28激活磁珠是主流的激活工具,其性能直接决定CAR-T细胞的扩增能力、阳性率、分化状态和耗竭水平,堪称 CAR-T制备的 “关键拼图”。长期以来,国内CAR-T产业使用的激活磁珠几乎被进口品牌垄断,不仅成本居高不下,还面临 “供货周期不可控” “国际物流风险” 等隐患。若能实现磁珠的国产替代,将为国内CAR-T产业按下 “降本提速” 的快进键。

数据说话:国产磁珠性能实测
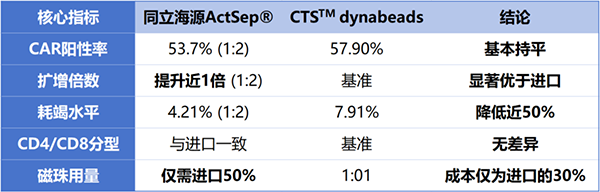
表格中”1:2”表示”CD3/CD28分选激活磁珠与CD3+T细胞的比例。数据来源于《中国肿瘤生物治疗杂志》2025年5月刊《国产与进口CD3/CD28激活磁珠制备CAR-T细胞的性能对比》。

性能达标只是基础,合规性才是国产磁珠进入临床应用的 “通行证”。同立海源ActSep®CD3/CD28分选激活磁珠(Cat.No. GMP-TL603)早已具备完善的合规资质:
符合GMP生产标准,生产与质量控制严格遵循ISO 9001和ISO 13485要求,支持药物申报;
已完成美国FDA的DMF备案(备案号:038124),国产磁珠不仅能替代进口,更能满足国际化的合规要求,为国内CAR-T企业出海铺路。

实现国产替代不仅是降低成本的需要,更是保障产业安全的战略选择!如果您正在开展CAR-T细胞研发或生产,不妨尝试使用同立海源ActSep®CD3/CD28分选激活磁珠,亲身体验国产替代带来的性能提升与成本优势。我们的技术团队将为您提供全方位的技术支持,确保您的实验顺利进行。


ActSep® CD3/CD28分选激活磁珠已经用于临床实验及相关申报。目前,获得审批的案例是北京艺妙医疗科技有限公司药品名称IM96嵌合抗原受体T细胞注射液(IM96 CAR-T细胞注射液)IND申报获批,CDE受理号CXSL2400463;以及北京艺妙医疗科技有限公司药品名称IM83嵌合抗原受体T细胞注射液(IM96 CAR-T细胞注射液)临床1期前物料变更申报获批,CDE受理号CTR20240565。
磁珠相关产品:
GMP级别分选、激活产品
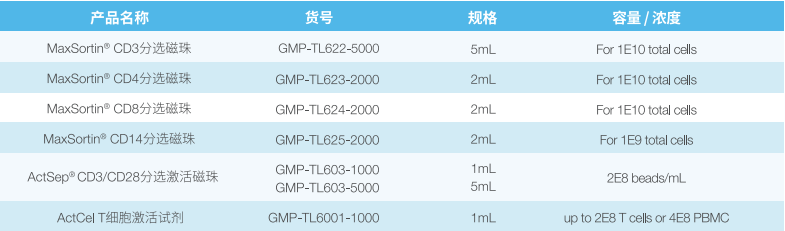
RUO级别分选、激活产品
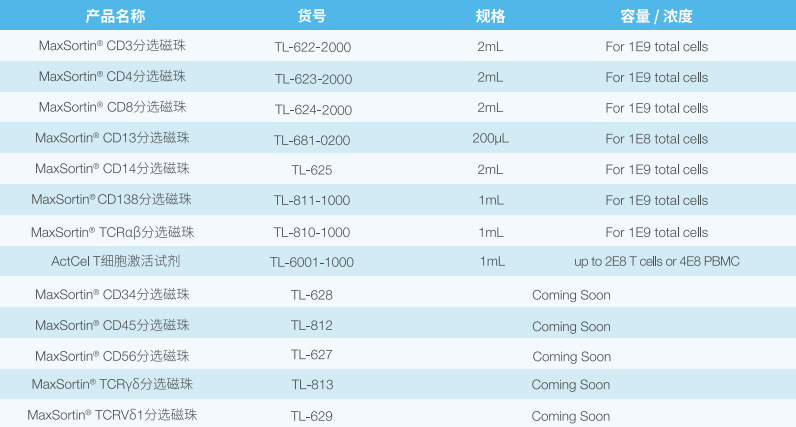
关于同立海源:
北京同立海源生物科技有限公司,专注细胞和基因治疗(CGT)GMP级原料试剂研发及生产,为CGT用户提供产品与服务的整体解决方案。产品涉及细胞分选磁珠试剂、重组人源蛋白、无血清培养基、细胞培养试剂盒等。
公司建有3400㎡的研发实验室及GMP级洁净车间,包括细胞分选磁珠开发平台、真核与原核蛋白表达工程平台、无血清培养基开发平台,通过ISO13485和ISO9001双质量体系认证,部分产品已获美国FDA DMF备案。