在现代医药飞速发展的今天,小分子药物和抗体药物已经完成了从横空出世到独领风骚的转变。问谁能继续引领现代药物研发的第三波潮流,那也只有核酸药物能扛得起这面大旗。核酸药物的研发周期短、作用效果直接且持久,不易产生耐药性。研发的底层逻辑在于依赖碱基互补配对原则,让药物直接作用于基因转录和翻译过程从根源上调控致病基因的表达,绕过了蛋白靶点难以成药的难题。核酸药物市场规模从0.1亿美金暴涨至的32.5亿美金,只用了短短五年时间。全球目前共有15款小核酸药物获批上市,包括9款ASO药物、5款siRNA药物以及1款核酸适配体药物。权威机构Evaluate Pharma 和 BCG 统计分析,2024 年全球核酸市场规模将会达到 86亿美元。

核酸药物家族目前包括反义核酸(Antisense oligonucleotide, ASO)、微小RNA(microRNA, miRNA)、核酸适配体(Aptamer)、小干扰RNA(small interfering RNA, siRNA)、小激活RNA(small activating RNA, saRNA)等不同类型。药物需要被递送至靶细胞后与靶标mRNA结合发挥作用。
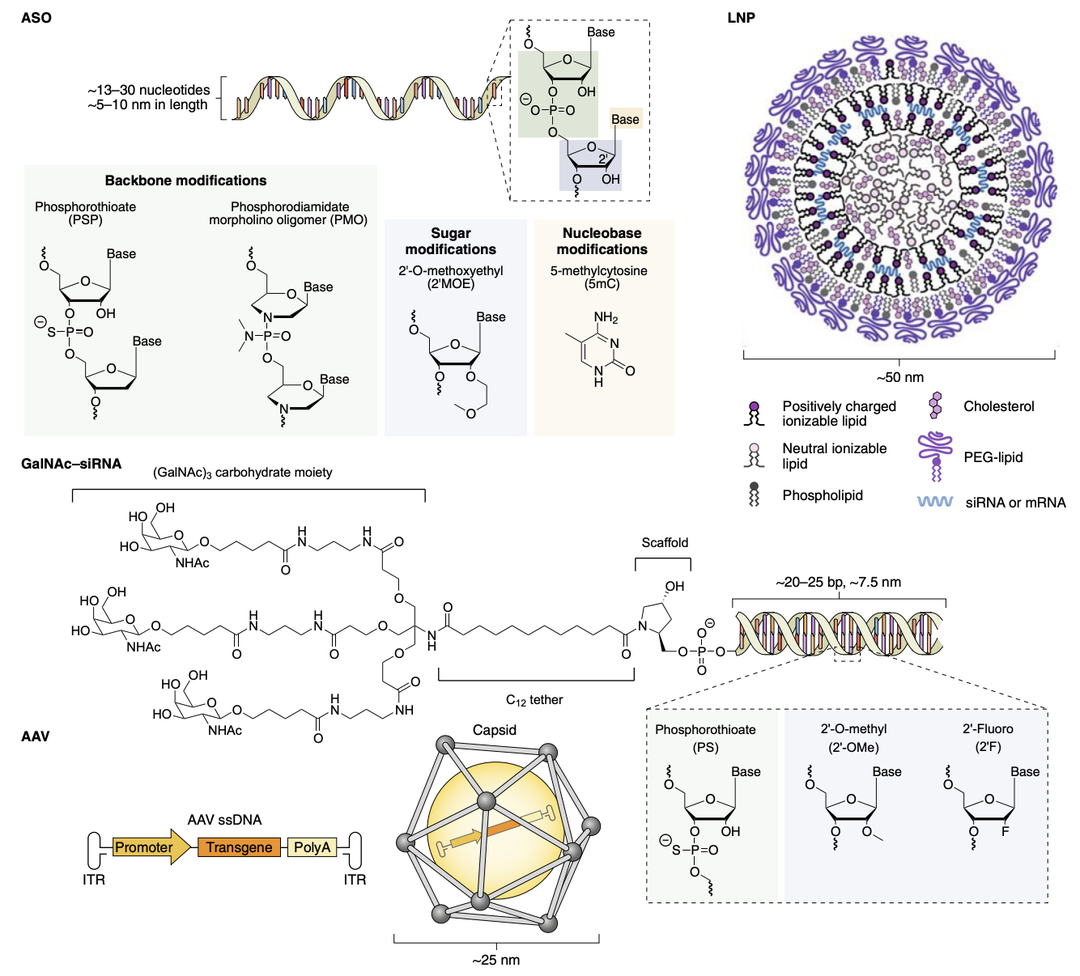
Fig1:核酸疗法目前依赖的四种平台技术
化学修饰可以对其药性产生重要影响,通常通过在核酸分子上引入不同的化学基团或结构来改变药物的性质、稳定性、药效和递送方式。我们可以通过药代动力学、药效学和生物分布等指标直观观察到修饰后带来的改善【1】。

Fig2:核酸药物的化学修饰方法
核糖-磷酸骨架修饰
核酸链的骨架修饰是通过在磷酸二酯键中引入硫代磷酸(PS)连接等方式,PS修饰可以降低药物的亲水性、增强抵抗核酸酶降解的能力、增加与血浆蛋白结合,从而提高药物的稳定性和半衰期【2】。PS修饰还可以促使小核酸药物在细胞核内富集,增强其与细胞内蛋白相互作用,从而增加药物的效果。然而,PS修饰也可能影响药物的活性和亲和力,因为硫原子引入的立体异构体可能导致不同的理化性质。在研发过程中,需要我们通过鉴定来选出最佳的立体异构体,这样后续的成药可以获得更有效的分子,同时也可以在一定程度上减少药物剂量。
核糖修饰
小核酸药物通常在核糖的2’位进行化学修饰,因为这样的修饰可以改变糖环的折叠结构,从而影响整个核酸分子的稳定构象,进而影响其结合能力和活性。同时,2’位的修饰还可以降低小核酸药物作为核酸酶底物的契合度,从而增强对核酸酶的抗性。最常用的2’位取代基包括2’-O-甲基(2’-OMe)、2’-O-甲氧基乙基(2’-MOE)和2’-氟(2’-F)。这些修饰可以提高药物在血浆中的稳定性,改善在组织中的半衰期,从而延长药物的作用时间【3】。
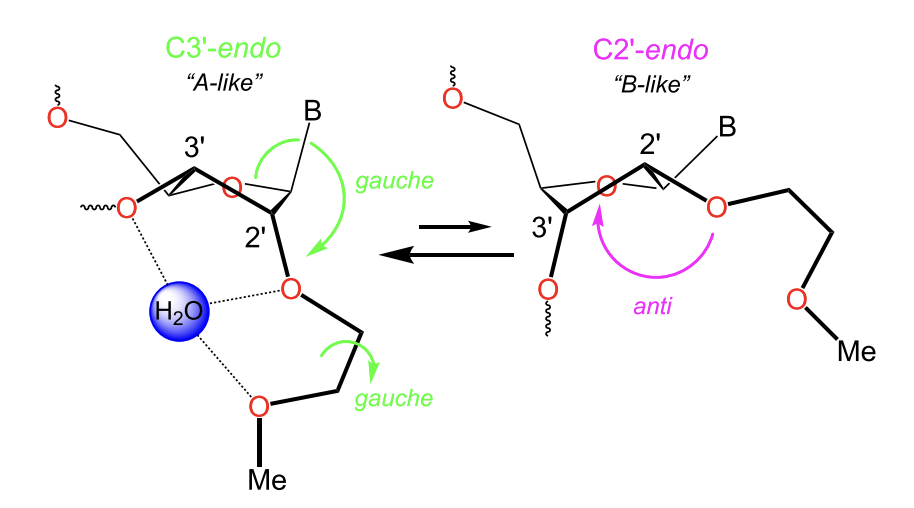
Fig3:2'- O -[(2-甲氧基)乙基]-RNA (MOE RNA)的加性变形
碱基修饰
小核酸药物主要通过与靶标序列碱基互补形成氢键发挥作用,因此碱基修饰可以改变两者间碱基配对的相互作用。在尿嘧啶的5位做替代是常用的碱基修饰策略。引入5-溴尿嘧啶、5-碘尿嘧啶可加强腺嘌呤-尿嘧啶(A-U)之间的连接,提高碱基的相互作用力,寡核苷酸与目标RNA 结合得紧密,则可以隐藏剪接位点,防止核糖体组装,最大限度的抑制翻译的发生。碱基修饰可以增强适体的 3D 结构,但是同时结合力的增强可能会增加脱靶结合的风险,从而增加不良反应的风险,在应用该技术时需要客观考虑现实状况。
末端修饰
末端修饰可用于靶向特定细胞类型或提高药物穿透细胞膜的能力,且核酸适配体、抗体、叶酸、N-乙酰半乳糖胺等结构也可用于末端修饰的靶向功能。最近上市的三款siRNA药物均采用GalNac修饰即N-乙酰半乳糖胺修饰,通过将GalNac以三价态的方式共价偶联至核酸3’末端,形成多糖-siRNA单缀合物【4】。

Fig4:GalNAc-siRNA靶向原理
选择合适的末端位置引入功能结构非常关键,通常在过客链的末端连接功能性分子,以保持向导链对靶标的沉默活性并减弱过客链引起的脱靶效应。同时,连接方式应选择可被切割或在酸性条件下不稳定的化学键,以便药物在细胞内裂解分离。
结语:化学修饰已经是一门较为成熟的技术,可选择的方案种类多、涉及的方面广,甚至可以协同合作,比如单个ASO药物经常包含多个修饰以结合其优势特性并减轻相关并发症。可以说它已经是科学家手头打磨核酸药物称手的“金刚钻”了,在小核酸药物蓬勃发展的今天,相信会在未来为我们带来更多的创新和突破。
转染技术作为核糖核酸干扰分子疗法(RNAi)药物的核心关键技术,选择转染试剂产品是否能够高效率的进行细胞转染及转染后的细胞毒性大小是首要考虑的问题,同立海源生物研发生产的LipidnanoTM Super RNAi 转染试剂(货号:TL-1001)独具核心竞争力,是一款高效能、非强正电型脂质转染试剂,用于siRNA介导的基因敲低实现,适合将siRNA和miRNA等小RNA高效地输送到广泛的细胞类型中。特有的超高细胞利用率,在低摄取量下即可达到高效的靶基因敲低水平,转染效果优于行业同类型竞品。另外公司还可提供小核酸药物递送服务,高效安全、精准靶向的递送系统提升RNAi治疗的有效性,助力突破小核酸药物递送壁垒。
● 高效低毒
● 操作简便
● 低摄取高表达,超高细胞利用率
● 适用于多种难转染细胞
● 易于实现体内转化
■ 高转染效率

图1:对多种常规细胞及难转染细胞均有较高的转染效率
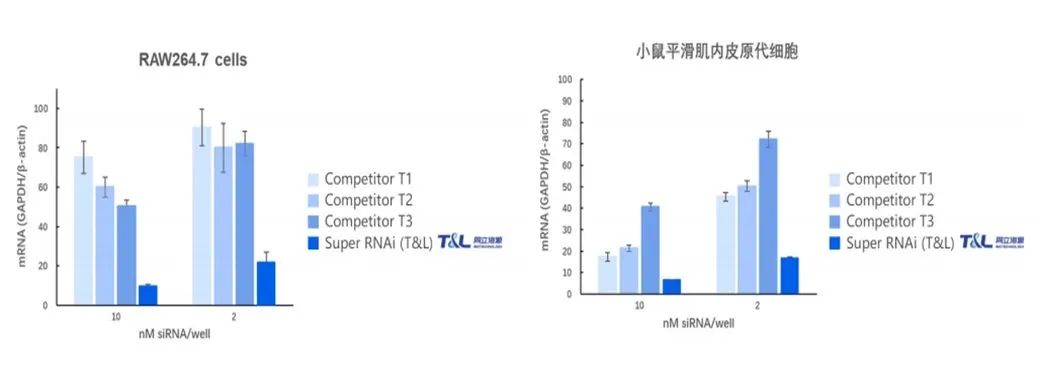
图2:对多种难转染细胞,具有高转染效率,并优于行业同类型竞品
■ 低细胞毒性
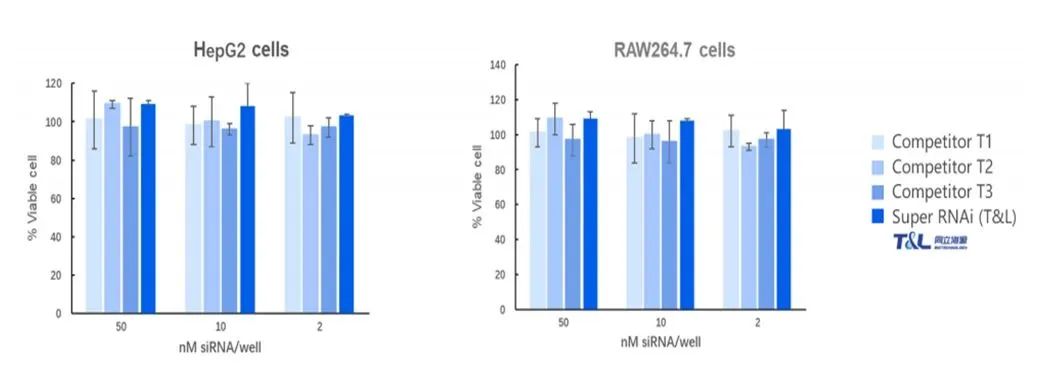
图3:LipidnanoTM Super RNAi 转染试剂在实现高靶基因抑制水平的同时,具有极低的细胞毒性
参考文献:
【1】 Zhu Y, Zhu L, Wang X, Jin H. RNA-based therapeutics: an overview and prospectus. Cell Death Dis. 2022 Jul 23;13(7):644.
【2】 Eckstein F. Phosphorothioates , essential components of therapeutic oligonucleotides. Nucleic Acid Ther. 2014 Dec;24(6):374-87.
【3】 Egli M, Manoharan M. Chemistry, structure and function of approved oligonucleotide therapeutics. Nucleic Acids Res. 2023 Apr 11;51(6):2529-2573.
【4】 Springer AD, Dowdy SF. GalNAc-siRNA Conjugates: Leading the Way for Delivery of RNAi Therapeutics. Nucleic Acid Ther. 2018 Jun;28(3):109-118.