
MSC疗法是一种细胞治疗技术,利用人体自身的干细胞进行治疗。MSC全称为间充质干细胞(Mesenchymal stem cells),是一类多功能干细胞,广泛存在于人体各种组织中。MSC具有自我复制、分化成多种细胞类型以及调节免疫反应等重要特性,因此被认为是一种极具潜力的治疗方法。
MSC疗法具有广泛的应用范围,可用于治疗心血管疾病、神经退行性疾病、创伤和炎症等多种疾病。具体来说,MSC疗法可以通过增强人体自我修复能力、调节免疫反应、减轻炎症反应、促进组织再生等作用,有效治疗各种疾病。
2018年度获批药物统计

2019年度获批药物统计
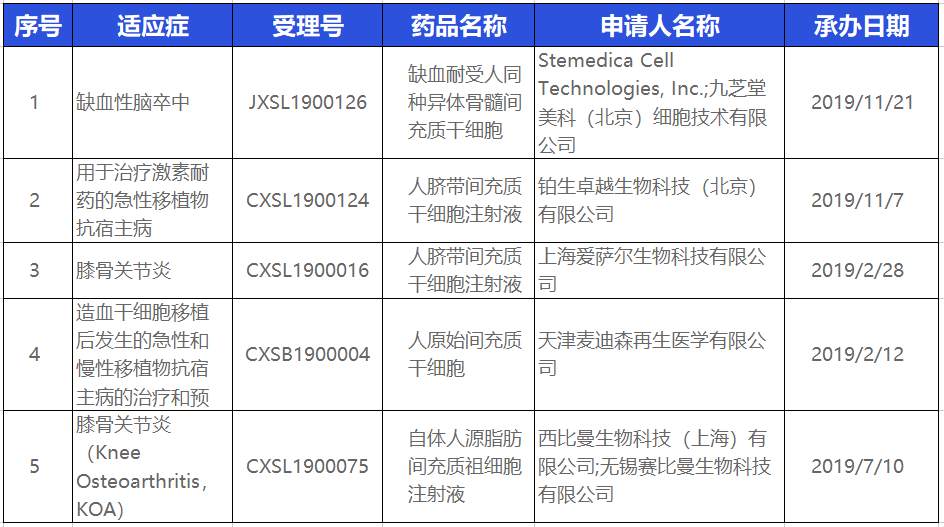
2020年度获批药物统计
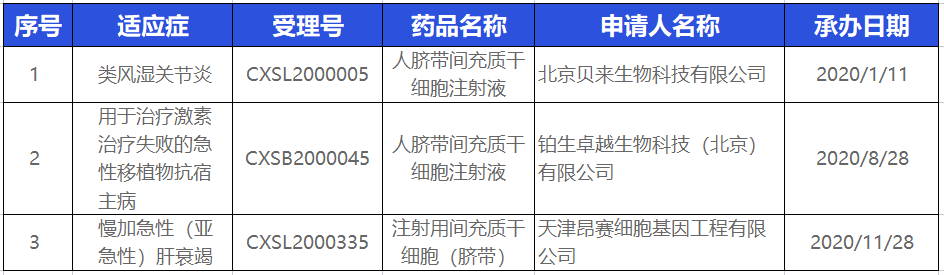
2021年度获批药物统计

2022年度获批药物统计
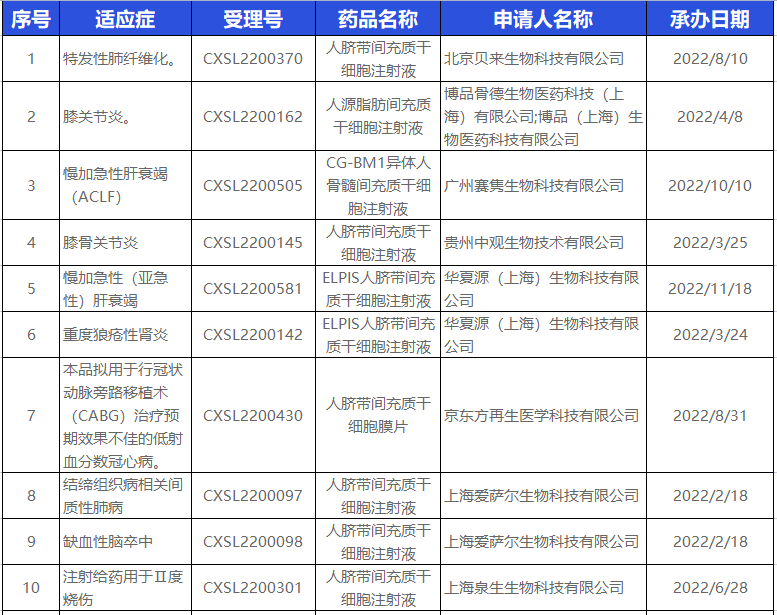
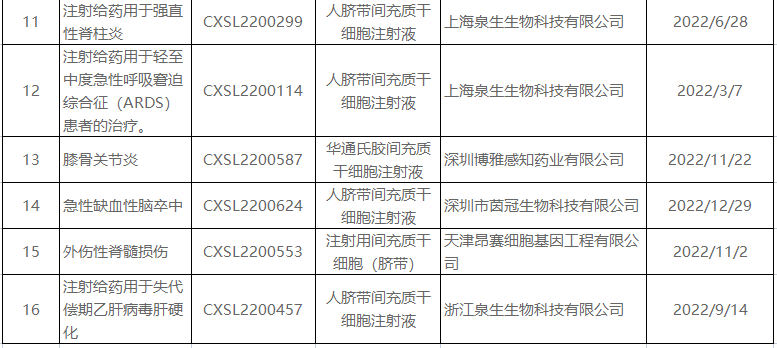
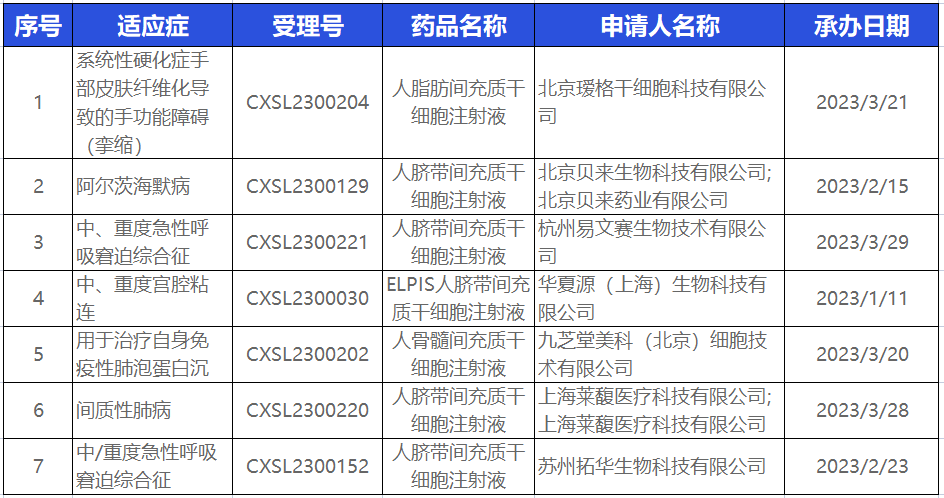
2023年度获批药物统计
自2017年国家食品药品监督管理总局颁布《细胞治疗产品研究与评价技术指导原则(试行)》以来,我国对于按照药品管理相关法律法规进行研发的细胞治疗产品的技术要求进行了总体阐述。随着干细胞技术的不断发展,相关产品的技术要求逐步修订和完善。最近,于2023年4月27日国家食品药品监督管理总局颁布了《人源干细胞产品药学研究与评价技术指导原则(试行)》,这一指导原则对于干细胞产品的药学研发和申报进一步规范和指导。这些指导原则强调了干细胞的特殊性质,强调在干细胞产品的生产工艺设计与验证、质量研究和控制、稳定性研究等研发过程中,应对各个环节的干细胞特性进行充分考虑。
目前,我国已有多款间充质干细胞药物通过新药临床研究审批(IND)进入临床试验阶段,这表明干细胞药物的研发和临床应用正逐步走向成熟。而随着干细胞技术研究的不断深入和经验的积累,相信未来会有更多针对新适应症的干细胞药物进入临床试验阶段,同时正在开展的干细胞药物Ⅰ期/Ⅱ期临床试验的研究也将逐步产生结果,这将有助于我们更好地了解干细胞的治疗效果和安全性。
随着政策法规的明确和干细胞技术的不断发展,干细胞作为治疗药物的应用前景日益广阔。政府和监管部门积极推动干细胞药物研发和临床应用的规范化和标准化,加强对干细胞药物生产、质量控制和安全性评估的监管和管理,为干细胞药物的上市提供了有力保障。同时,企业也在不断加大研发投入,探索新的治疗应用领域,不断推动干细胞技术的创新和进步。虽然干细胞药物的研发和临床应用仍存在一些挑战和风险,如研发周期长、生产成本高、安全性难以保证等,但随着行业的进步和不断的探索,这些难题将得到逐步解决。相信在监管部门、企业、科研机构和医疗机构的共同努力下,干细胞药物的临床应用将会得到更广泛的应用,为中国的医药事业发展注入新的动力。
同立海源AMMS®MSC试剂盒套装已通过美国FDA DMF II类备案(备案号:035589),该款试剂盒化学成分明确,无血清,含有多种氨基酸、微量元素等,操作简便,适用于人间充质干细胞原代及传代培养,支持干细胞药物申报。



MSC扩增后表型
