

近些年来,随着细胞生物学、免疫学和合成生物学技术壁垒的不断突破,有力地支撑了细胞治疗技术和细胞治疗产业的快速发展。细胞治疗,是指利用某些具有特定功能的细胞特性,采用生物工程方法获取和/或通过体外扩增、特殊培养等处理后,产生特异性功能强大的细胞,回输体内后达到治疗特定疾病的目的。目前主要的细胞治疗方式为免疫细胞治疗和干细胞治疗,而基因治疗技术也穿插应用于免疫细胞和干细胞治疗技术之中。
细胞治疗药物市场现状
细胞疗法作为创新生物技术在医疗健康发展中扮演着重要角色。一方面,当下小分子、单抗、双抗等技术在部分癌种上已经出现有效性瓶颈, 颠覆性改变患者治疗现状亟待新的创新技术的出现;另一方面,创新技术的产业环境亟待新的底层逻辑挖掘,区别于过去传统治疗方案的市场评估体系,细胞治疗作为技术和消费属性并存的创新治疗方案,其技术的高壁垒性决定了我们应当以新的逻辑思维去审视整个行业的发展。
美国哈佛大学的乔治戴利教授说过:“如果20世纪是药物治疗的时代,那么21世纪就是细胞治疗的时代!”理想化的细胞治疗技术相较于传统治疗手段有着诸多优势(更精准、更高效、更少副作用等),在这些理念的驱使下,最近一二十年来,许多药企在资本的推进下,加快了细胞治疗药物的上市应用速度。中国的细胞治疗产业起步晚,但是随着欧美生物医药技术人才的“回流”和国内经济的快速发展,细胞治疗产业作为新型生物医药产业的核心组成部分也获得了资本的青睐,成为当前的热门投资方向。
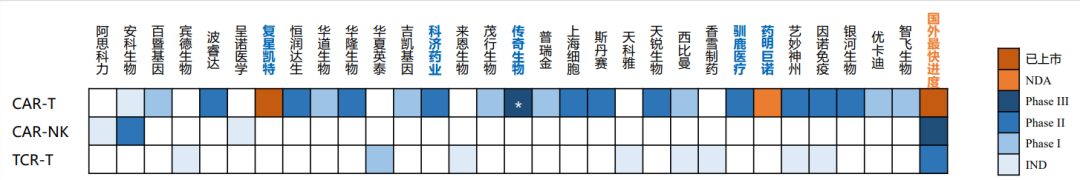
中国细胞治疗产业公司布局(图源东吴证券)
* 目前在研的CAR-T中,国内临床研究以Phase II作为关键性试验, Phase III为产品在美进度
CAR-T技术是当前国内市场独有上市的细胞治疗产品:2021年,中国NMPA批准两款CAR-T上市;2022年2月,南京传奇研发的CAR-T产品 cital-cel成功在美国上市销售。许多靶点为免疫细胞共有,因此,CAR-T、CAR-NK、TCR-T和CAR-M等都会成为不同公司研发管线的布局组成部分。
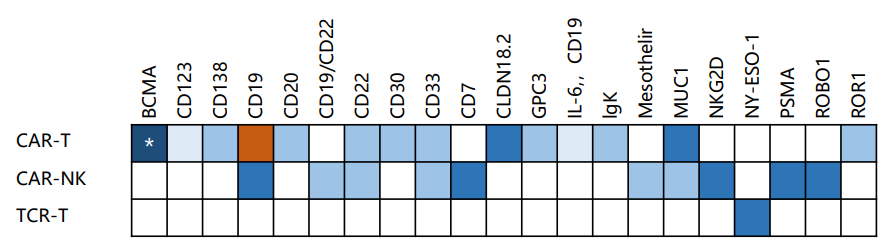
中国细胞治疗产业靶点布局(图源:东吴证券)
* 目前在研的CAR-T中,国内临床研究以Phase II作为关键性试验,Phase III为产品在美进度
细胞治疗药物质控
细胞治疗产品从研发到上市的路径十分复杂,对于原料、生产环境、生产工艺、临床试验和上市许可申请等各个部分的要求都十分严格。在美国,根据《公共卫生服务法》 (PHS Act; 42 U.S.C. 262) 第351条的规定,经过培养扩增的 MSCs 产品需要向 FDA 提交 IND 申请,获得许可开展临床试验;在欧盟,基于 MSCs 的治疗产品开发和授权由欧洲药品管理局 (EMA) 监管;EMA还为此成立了高级治疗委员会 (CAT),负责 MSCs 治疗产品的审评和许可;在中国,根据现行监管法规,在临床研究中使用 MSCs 可通过两种途径获得许可。其一,卫健委已经实施了细胞治疗产品开展临床研究的相关法规,批准通过伦理委员会审查合格的指定医院,进行 MSCs 临床研究。其二,如果申办者打算开发 MSCs 药物,则使用 MSCs 产品的临床试验需要根据 NMPA 法规获得CDE规定的 IND 申请并获得许可。近年来,国家药监局改革举措不断,其中不得不提的一点就是新药临床默示审批制度,这也为国内干细胞新药的开发提供了有力的支持和保障。IND 申请必须由申请人提交,并提供全面的信息 (包括细胞和制造工艺的开发、质量标准、质量控制、MSCs产品的稳定性研究、药效研究、安全性和毒性研究以及临床试验计划和试验方案)。根据 我国IND 申报的规定,MSCs 产品必须在符合 GMP标准的实验室内生产。
我国政府对于细胞治疗类产品的质量要求历来非常重视,出台了多项细胞治疗制品质量相关的政策:1993年,《人体细胞治疗及基因治疗临床研究质控要点》;2009年,《自体免疫细胞(T细胞、NK细胞)治疗技术管理规范》(征求意见稿),《细胞移植治疗技术管理规范》(征求意见稿);2013,《干细胞制剂质量控制及临床前研究指导原则(试行)》(征求意见稿);2015年,《干细胞制剂质量控制及临床前研究指导原则(试行)》;2017年,《干细胞通用要求》,《总局关于发布细胞治疗产品研究与评价技术指导原则的通告(2017年第216号)》;2018年,《嵌合抗原受体修饰T细胞(CAR-T细胞)制剂制备质量管理规范》;2021年,“免疫细胞治疗产品临床试验技术指导原则(试行)”、“药品生产质量管理规范-细胞治疗产品附录(征求意见稿)”;2022年,“嵌合抗原受体修饰T细胞(CAR-T细胞)制剂制备质量管理规范”等。
细胞治疗制品生产时所涉及的生产材料主要是指用于制备细胞治疗产品的物质或材料,包括细胞、培养基、细胞因子、各种添加成分、冻存液、基因修饰/改造用物质和辅料等。生产用材料直接关系到产品的质量,因此研究者应建立良好、规范的生产用材料的质量管理体系,包括使用风险的评估、对关键生产用材料的供应商审计和制订质量放行检测机制等工作程序。
细胞治疗药物原材料具体要求
细胞制品原材料的选择是基于风险评估的原则,通过风险评估从而建立与之相应的风险控制策略,通常会有以下几种考虑:
1、在产品研发早期就开始设计所用原材料的类别并分析其可能的风险,可根据我国现行版《中国药典》三部中“生物制品生产用原材料及辅料质量控制规程”及国外相关技术要求对原材料的风险等级进行评估并分类,同一种试剂或材料,优先选择低风险级别的,如药用无菌制剂优于药用制剂,药用级优先于非药用级、GMP级优先于非GMP级、非动物源性优先于动物源性材料等;
2、根据对每一种原材料风险评估的结果建立相应的质量检测项目、检测方法及放行标准,并在产品研发过程中不断分析关键原材料质量对产品质量的影响,并不断改进关键原材料的质量要求;
3、对于研究级别的生物源性的原材料,不仅要设置它们的安全性质控项目,如无菌、内毒素、支原体、分枝杆菌及外源病毒污染的检测等,还要考虑它们的纯度、效价或对细胞活化、增殖的生物学效力的质控项目。动物源性材料的质量控制,如牛血清,需至少按照已有的国家标准或要求进行原材料质控及放行;
4、对于自行研制的原材料,如某种特殊要求的细胞因子,不仅需要建立质量标准,还需要有制备工艺及其工艺验证等数据支持,有的高风险的原材料甚至可能还会要求开展动物体内的安全性评估。此类原材料的检测要求需要根据其使用方式、下游工艺的清除验证数据以及潜在风险来确定。辅料的选择及控制要求同样是基于风险评估的原则,因辅料是和CAR-T产品一同进入患者体内,因此,选择低风险的辅料以及严格控制辅料风险是基本原则,如一种辅料同时存在几种风险等级来源时,应选用风险等级低的辅料;对于高风险等级的辅料,应在产品研发的早期评价使用这些辅料的必要性, 并寻找其他替代物或替代来源。
结语
虽然目前细胞治疗制品在临床试验中总体表现出较好的安全性,但是除了生产工艺复杂、质量影响因素众多外,还存在不少制约其商业化发展的不利因素。总之,我国的细胞治疗类生物制品的商业化成药研发还处在起步阶段,研发者对按药品管理的细胞产品研发思路和质量控制策略还缺乏深入的研究,监管机构对于细胞产品的理解和认识也在累积的过程中。我们相信,随着科研水平的进步和细胞治疗技术的不断成熟,在细胞治疗领域的临床表现和应用前景将逐步明朗!
关于同立海源
北京同立海源生物科技有限公司,专注细胞和基因治疗(CGT)上游GMP级原料试剂研发及生产,为CGT用户提供产品与服务的整体解决方案。产品涉及细胞分选磁珠试剂、真核/原核重组蛋白、无血清培养基、细胞培养试剂盒等。
公司建有3200㎡的研发实验室及GMP级洁净车间,包括细胞分选磁珠开发平台、真核与原核蛋白表达工程平台、无血清培养基开发平台,通过ISO13485和ISO9001双质量体系认证,部分产品已获美国FDA DMF备案。
